Alpha-1-Antitrypsin Mangel: Seltene Mutationen
AutorIn
Dipl.-Biologin Martina Veith, PD Dr. med. Timm Greulich
Die Ursache für den Alpha-1-Antitrypsin-Mangel (AAT-Mangel) sind Mutationen (Veränderungen) im SERPINA1-Gen (Serin-Protease-Inhibitor A1-Gen), welches sich auf dem Chromosom 14 befindet. Das AAT-Gen weist eine beträchtliche genetische Variabilität auf. Mittlerweile sind über 100 verschiedene Mutationen des SERPINA1-Gens bekannt, darunter auch viele seltene Mutationen, die zu Strukturveränderungen von AAT führen können und somit Krankheitsbilder unterschiedlichen Schweregrades haben können. Mutationen dieses Gens können, müssen aber nicht zum Mangel an AAT führen. Je nach Art und Stelle der Mutation auf dem SERPINA1-Gen ist das AAT-Protein in der Funktion mehr oder weniger eingeschränkt bis hin zum kompletten Fehlen des AAT-Proteins. Bei manchen Mutationen, z. B der häufig auftretenden Z-Mutation, kommt es zu einer Anhäufung des Moleküls in der Leber und dadurch zu einem Mangel von AAT im gesamten Organismus, wodurch die Schutzfunktion (enzymatischer Abbau von Lungengewebe) nicht mehr oder nur noch teilweise erfüllt wird. Dies kann zu einer Funktionsstörung verschiedener Organe, insbesondere der Leber und Lunge führen. Die AAT-Allel-Varianten werden in Gruppen eingeteilt: Normal (Pi*M-Allel) = normaler AAT-Serumspiegel, Defizienz = signifikante Reduktion des AAT-Serumspiegels, Null (Q0) = kein AAT nachweisbar. Die unterschiedlichen Mutationen werden mit Buchstaben von A-Z und Null (Q0) bezeichnet und richten sich nach der Wanderungsgeschwindigkeit bei der pH-Wert-abhängigen elektrophoretischen Auftrennung des Alpha-1-Proteins. Das normale (gesunde) Allel wird als M bezeichnet (Abb.1). Da das Genom des Menschen aus einem doppelten Chromosomensatz besteht, bezeichnet die Formel Pi*MM einen gesunden Menschen ohne Mutation (Pi steht dabei für Protease-Inhibitor, die beiden folgenden Großbuchstaben geben den Zustand der beiden Allele an). Es wird zwischen homozygoten, heterozygoten und compound heterozygoten Formen unterschieden. Homozygot meint, dass beide Allele identisch sind, im Falle einer Krankheit also beide Allele dieselbe krankmachende Mutation aufweisen (z.B. Pi*ZZ). Bei der heterozygoten Form ist hingegen nur eine Genkopie (Allel) von der Mutation betroffen, die andere liegt unverändert vor (z.B. Pi*MZ). Bei der compound heterozygoten Mutation befinden sich zwei unterschiedliche Mutationen auf beiden Allelen (z.B. Pi*SZ). Die meisten seltenen Mutationen haben zusätzlich zu dem Buchstaben noch einen Namen, der sich nach dem Geburtsort des Patienten oder nach dem Ort bzw. dem Institut richtet, wo die Mutation als erstes entdeckt wurde, z.B. Pi*MWürzburg, Pi*LOffenbach, Pi*YBarcelona, Pi*Q0Mattawa. Es gibt einige sehr seltene Mutationen, die bis jetzt nur einmal detektiert wurden. Bei manchen dieser Mutationen wurde kein Name vergeben, hier wird nur die genaue Stelle der Mutation auf dem Gen angegeben, z.B. c.221T > A.
Nach wie vor ist über die Epidemiologie der seltenen AAT-Varianten wenig bekannt. Die Ergebnisse aus dem Marburger Alpha-1-Labor zeigen nur bei 1 % der Einsendungen seltene Varianten, so dass man ein sehr seltenes Vorkommen in der Bevölkerung annehmen muss (Abb. 2). Eine gute Diagnostik ist wichtig, um seltene und auch zuvor noch nie beschriebene Mutationen detektieren zu können. Verschiedene Analysen, wie die Bestimmung des AAT-Serumspiegels, die Genotypisierung (auf DNA-Ebene, Screening der 14 häufigsten und seltenen AAT-Mutationen), Phänotypisierung (auf Protein-Ebene), und ggf. die Sequenzierung (auf DNA-Ebene, kompletter kodierender Bereich) stehen dafür zur Verfügung. Der AAT-Serumspiegel ist bei der Detektion von seltenen Mutationen unerlässlich und ist darüber hinaus zur klinischen Wertung der detektierten Mutationen sehr wichtig. In den meisten Fällen können seltene Mutationen nur durch die Auswertung der verschiedenen Methoden entdeckt werden. Der klinische Verlauf bei seltenen AAT-Mutationen ist aufgrund der sehr geringen Patientenzahl schwer zu beurteilen. Um hierzu einen besseren Überblick zu erlangen, werden aktuell Fragebogenaktionen durchgeführt. Bei vielen seltenen Mutationen kann aufgrund der fehlenden Vergleichbarkeit keine Aussage zu dem Krankheitsbild getroffene werden. Bei einer seltenen Krankheit wie dem Alpha-1-Antirypsinmangel ist es wichtig, dass das Expertenwissen zusammengefügt wird und somit ein Vergleich und Austausch stattfinden kann. Einer der wichtigsten Ziele der aktuellen Forschung ist es daher, Vergleichbarkeiten zu finden, um die unterschiedlichen Verläufe trotz gleicher Mutationen verstehen und zielgerichteter behandeln zu können.
Mit einer Teilnahme an dem Fragebogen können Patienten einen aktiven Beitrag zur Forschung und zum besseren Verständnis der Erkrankung leisten, was wiederum den Betroffenen zu Gute kommt.

Abbildung 1: pH-Wert abhängige elektrophoretische Auftrennung von den unterschiedlich mutierten Alpha-1-Proteinen (A-Z). Das normale (gesunde) Allel wird als M (M1-M4) bezeichnet (Ignacio Blanco. Blanco’s Overview of Alpha-1 Antitrypsin Deficiency. 2017, S.108).
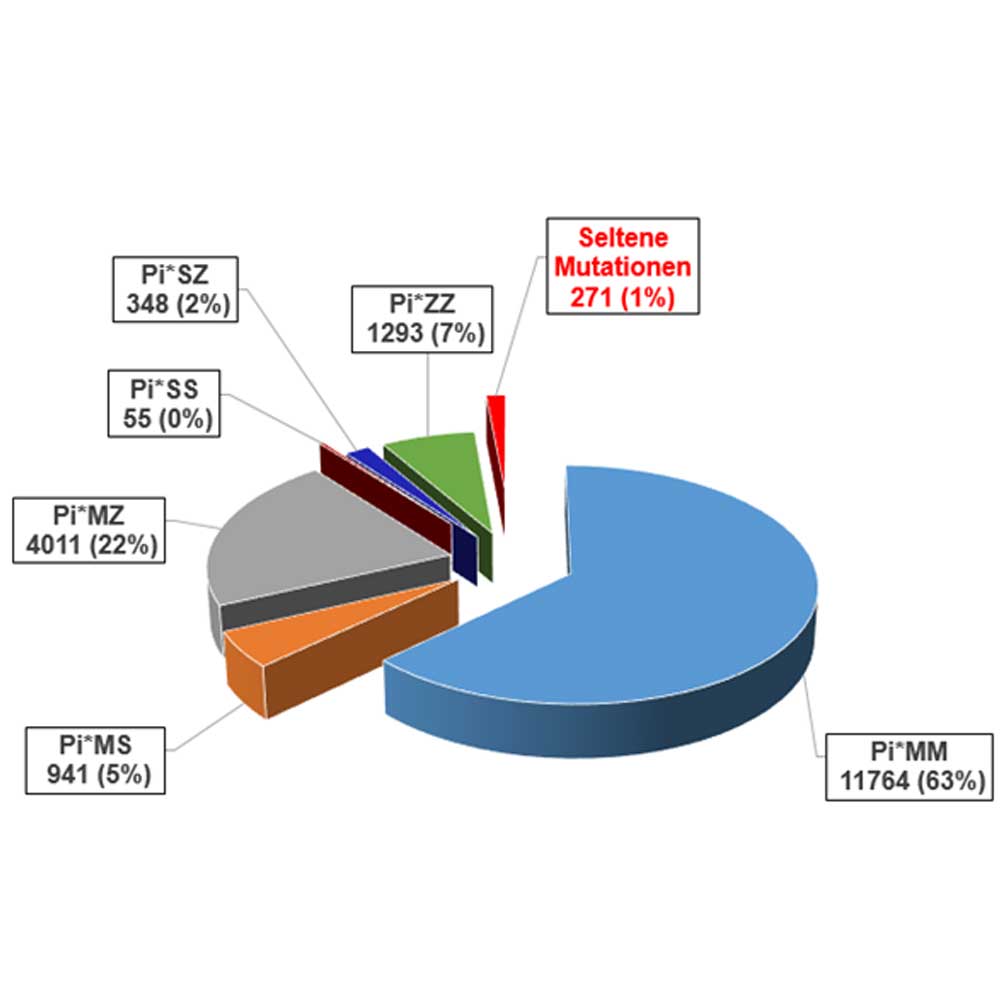
Abbildung 2: Verteilung der Mutationen bei einer Anzahl von insgesamt 18683 Patienten (Pi*MM=Gesund) (Greulich et al. Results from a large targeted screening program for alpha-1-antitrypsin deficiency: 2003 – 2015. Orphanet Journal of Rare Diseases 2016; 11:75).
Weg mit der Frühjahrsmüdigkeit und ran an den Frühjahrsputz!
Eigentlich passt der Frühjahrsputz gut zu unserem Motto 2019 „runter vom Sofa rein ins Leben“, aber wussten Sie, dass wir Lungenerkrankten eine gute Ausrede haben, es mit dem Putzen nicht zu übertreiben?
So manche Reinigungsmittel gehen nicht nur dem Dreck an die Gurgel sondern landen in Form von Dämpfen ebenfalls in unsere Lunge und schädigen diese. Neben Luftnot sind Allergien und Hautschädigungen ein Problem beim Putzen.
Einer Studie der norwegischen Universität Bergen nach sind Frauen, die regelmäßig putzen oder beruflich reinigen, langfristig öfters von einem starken Abfall der Lungenfunktion betroffen. Die Daten wurden im American Journal of Respiratory and Critical Care Medicine veröffentlicht.
Zum Weiterlesen haben wir folgende links für Sie entdeckt:
Schon gewusst:
797 Organspender gab es in Deutschland 2017, fast 500 weniger als 7 Jahre zuvor. Obwohl 84 der Deutschen die Bereitschaft zur Organentnahme erklären haben nur 36 einen Organspendeausweis. (Quelle: Apotheken Umschau 01/2019)

Einführung eines ABCs der Leber
Autor: Alexander Niepel, Gruppenleiter der SHG München
Wenn’s der Leber gut geht merkt man von ihr nichts, ebenso wie von vielen anderen Organen. Das Tückische ist, dass man bei der Leber auch bei Erkrankungen häufig erst spät etwas merkt. Wenn die Leber, zum Beispiel durch einen AAT-Mangel, betroffen ist, steht man schnell vor einem Berg an Begriffen, die für Laien im Grunde nicht fassbar sind. Als Betroffener versuche ich ein paar Fachbegriffe so einzuordnen, wie ich ihnen begegnet bin.
>>> Lesen Sie den ganzen Artikel auf unserer Internetseite.

